Investigadores santafesinos monitorean la aparición de nuevas cepas de covid en el país

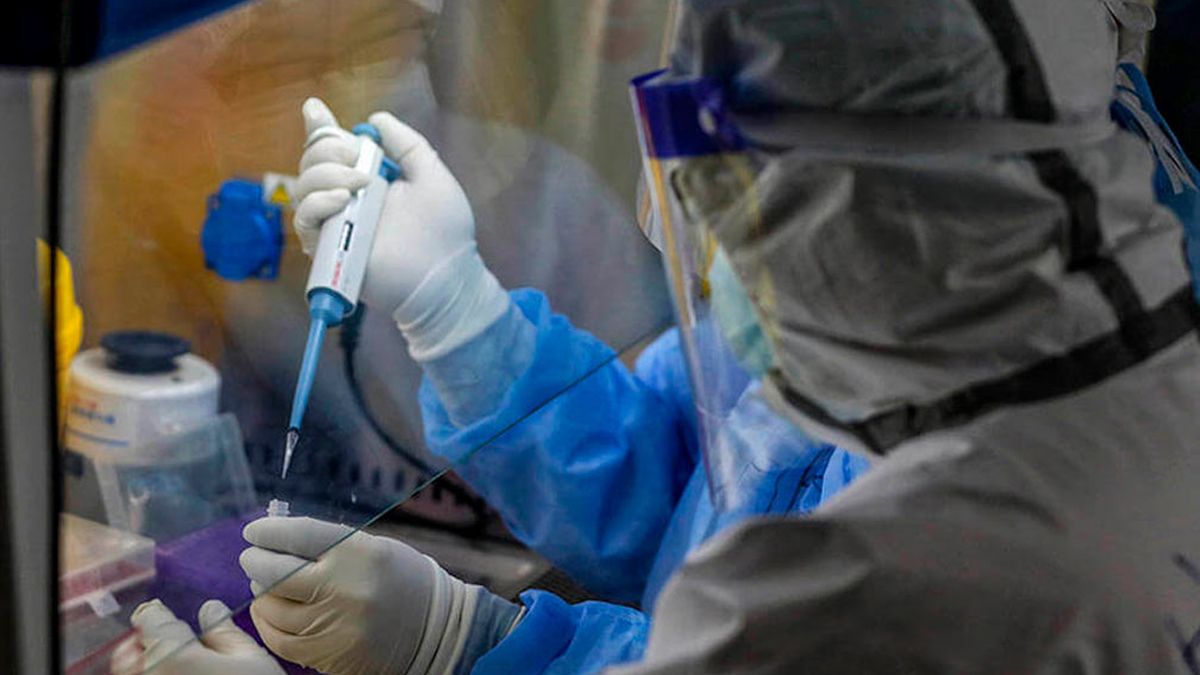
Investigadores santafesinos del Instituto de Investigación de la Cadena Láctea del Inta-Conicet de Rafaela, que integra el Conicet Santa Fe, participan en la vigilancia de presencia de variantes de coronavirus en el país. Es en el marco del proyecto “Genómica de los virus SARS-CoV-2 productores de COVID-19 en Argentina. Análisis integral de aspectos genéticos, clínicos y evolutivos de cepas autóctonas y su impacto en el diagnóstico y la epidemiología local y global”, una de las 64 iniciativas seleccionadas de la Convocatoria IP COVID-19 que financia la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación (Agencia I+D+i) en el marco de la Unidad Coronavirus integrada junto con el Ministerio de Ciencia, Tecnología e Innovación de la Nación y el Conicet.
Te podría interesar
El proyecto, dirigido por Mariana Viegas, se propone brindar conocimiento actualizado de las diferentes variantes que circulan en nuestro país a través de la obtención de secuencias de genomas de SARS-CoV-2, análisis filogenéticos, filogeográficos y de asociación clínico-epidemiológicos derivados.
Una nueva herramienta frente a la aparición de nuevas variantes de COVID-19
La emergencia de variantes virales es un proceso natural de la evolución de los virus. Durante la última quincena de diciembre de 2020, tres variantes virales del SARS-CoV-2 despertaron la atención de la comunidad científica y de los gobiernos nacionales: las variantes VOC 202012/01 (linaje B.1.1.7), cuya muestra más reciente fue detectada en el Reino Unido el 20/09/2020; la variante 501Y.V2 (linaje B.1.351), detectada en Sudáfrica desde el 08/10/2020, y la variante de Río de Janeiro (derivada del linaje B.1.1.28), detectada Río de Janeiro, Brasil, desde octubre de 2020.
Cuando las variantes se presentan con cambios genéticos en regiones geográficas con circulación del virus es preciso evaluar el posible impacto de esos cambios genéticos sobre la propagación viral, la capacidad de causar enfermedad más severa o la respuesta a la vacunación.
Para determinar la posible circulación de estas variantes en nuestro país, se requiere una vigilancia activa de las variantes genéticas del SARS-CoV-2, ya sea a través de la secuenciación del genoma completo, o mediante el análisis de secuencias parciales que incluyan marcadores genéticos de interés. “Desde el proyecto ideamos una metodología para determinar en forma más rápida si estas variantes pudieron haber ingresado a nuestro país en algún momento a través de algún viajero. La estrategia consiste en secuenciar un fragmento pequeño que nos permite hacerlo más rápido sin necesidad de juntar gran cantidad de muestras para poder procesar en tiempo real” explica Viegas.
Aplicando esta metodología, el Consorcio Argentino Interinstitucional de Genómica de SARS-CoV-2, a través los Nodos de Secuenciación del IDICaL del INTA-CONICET de Rafaela (Provincia de Santa Fe) y del Laboratorio de Virología del Hospital de Niños Ricardo Gutiérrez (CABA), realizó la secuenciación de genomas completos de SARS-CoV-2 procedentes de virus detectados en la ciudad de Santa Fe, CABA y Gran Buenos Aires entre un rango del 10 al 26 de diciembre de 2020. Todas las muestras correspondían a casos de circulación comunitaria.
Si bien el monitoreo es continuo, desde que comenzó la vigilancia activa de las variantes de interés de SARS-CoV-2, no se ha detectado aún ninguno de los cambios marcadores de la proteína S de la variante de Reino Unido.
La relevancia del monitoreo de las mutaciones en regiones específicas de la proteína S radica en que el dominio de unión al receptor (RBD) es el principal blanco de los anticuerpos neutralizantes que aparecen durante la infección por SARS-CoV-2. “Este tipo de vigilancia sobre mutaciones sirve como una especie de base de datos genómico local de las variaciones de los coronavirus locales” destaca la investigadora.
Contar con vigilancia rápida y ágil se presenta como un elemento estratégico para dar una respuesta adecuada a la pandemia. “Es clave entender qué sucede en tiempo real en la interacción entre los virus que circulan en nuestro país y las vacunas para estar alertas si acaso emerge una variante viral que es resistente a las mismas”, menciona Viegas entre los beneficios que brinda la herramienta.
Avances y desafíos del proyecto
Entre los avances más importantes del proyecto se destacan el desarrollo de una plataforma de difusión de resultados para la comunidad científica, la articulación con más de 40 laboratorios epidemiológicos de todo el país, la realización de protocolos para la secuenciación de los genomas virales, la determinación de los pasos bioinformáticos para el análisis de datos y la determinación de pautas de muestreo según la situación epidemiológica de las regiones estudiadas. Con este proyecto se logró obtener 613 genomas y se realizaron los análisis filogenéticos necesarios para poder determinar las distintas introducciones virales y el análisis de circulación local o comunitaria.
Uno de los agregados de valor del proyecto es la generación de datos en tiempo real. Desde el equipo de investigación han articulado con Inmunova, los desarrolladores del suero equipo hiperinmune (otro proyecto seleccionado y apoyado por la Agencia I+D+i en la Convocatoria IP COVID-19) para acceder a la base de datos en tiempo real, poder detectar posibles mutaciones y mejorar la efectividad del tratamiento. La información generada por el equipo de investigación está también disponible para los desarrolladores de kits de diagnóstico locales y para los grupos que están desarrollando vacunas.
Acerca del proyecto
Esta iniciativa fue evaluada y seleccionada por la Agencia I+D+i en el marco de la Convocatoria IP COVID-19 en el mes de abril de 2020. El organismo financió el proyecto a través del FONARSEC. “El apoyo fue fundamental porque si no teníamos financiación no podíamos desarrollar todo este gran consorcio que hoy en día está funcionando de manera articulada y colaborativamente”, afirmó Viegas. Además, el proyecto de análisis de muestras de Santa Fe, recibió financiamiento de COFECyT Federal SF-12 "Análisis de genomas completos del virus SARS-Cov-2 circulante en la provincia de Santa Fe en 2020".
En diciembre del año pasado, Viegas y su equipo fueron distinguidos por Google con su Premio de Investigación para América Latina debido a su alto impacto en la búsqueda de soluciones para los desafíos de la región a través del uso de la tecnología.
El objetivo inicial de este proyecto es caracterizar las distintas variantes del virus SARS-CoV- 2 que circulan en Argentina a través de la secuenciación de su genoma completo. “Uno de los objetivos que nos propusimos es descentralizar la secuenciación y poder responder a nivel local. Articular los nodos de secuación que están actualmente distribuidos en diversas provincias fue un desafío en una primera etapa”, destaca Viegas. Como resultado, se utilizan muestras provenientes de los centros de diagnóstico localizados en distintos puntos del país (CABA, provincia de Buenos Aires, Neuquén, Tierra del Fuego, Rio Negro, Córdoba y Chaco) para evaluar posibles cambios en el genoma que puedan afectar el diagnóstico o la respuesta al tratamiento.
Durante la etapa inicial de la pandemia, el proyecto se propuso identificar las distintas rutas de acceso por las que el virus ingresó a nuestro país a través de los pacientes con antecedente de viaje a zonas ya afectadas por COVID-19. En la siguiente etapa, se analizó la circulación viral autóctona o comunitaria y el establecimiento de circuitos locales de transmisión mediante una integración de la información epidemiológica y genética. En paralelo, se avanzó en la comparación de la distribución de las variantes del virus en distintas regiones geográficas de nuestro país, a distintos tiempos permitiendo rastrear su diseminación a lo largo del país. Se planea realizar estudios de correlación de las variantes del genoma del virus con la manifestación clínica de COVID-19 en función de parámetros como el grado de severidad, carga viral, etc.









